うつ病治療薬「レメロン®錠/リフレックス®錠」の製造販売承認取得のお知らせ
シェリング・プラウ株式会社(本社:大阪市中央区 社長:鳥居正男)と明治製菓株式会社(本社:東京都中央区 社長:佐藤尚忠)は、本日、両社で共同開発したうつ病治療薬「レメロン® 錠(シェリング・プラウ株式会社)/リフレックス® 錠(明治製菓株式会社)」(一般名:ミルタザピン)の製造販売承認を取得いたしましたのでお知らせいたします。
「ミルタザピン」はN.V.オルガノン社*注1 が創製したうつ病治療薬で、1994年に製品名『REMERON®』としてオランダで発売されて以来、現在では世界90ヵ国以上で販売されています。また、その特徴的な作用メカニズムによって、海外では『ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA: Noradrenergic and Specific Serotonergic Antidepressant)』というカテゴリーに分類され、選択的セロトニン再取り込み阻害薬(SSRI)やセロトニン・ノルアドレナリン再取り込み阻害薬(SNRI)とは異なる作用機序を持つ薬剤として知られています。
日本における臨床試験では、この領域では実施することが難しいとされているプラセボ対照比較試験において、投与1週目から有意な改善効果が示され、日本で初めてプラセボに対して抗うつ効果における優越性が検証されました。また、長期投与試験においては、 52週まで抗うつ効果が維持されることも示され、効果の早期発現と長期維持などの特長を持ち合わせた薬剤です。今回の承認取得により、本剤がうつ病における薬物治療の新しい選択肢として、患者さんのQOL向上に貢献できるものと期待しています。
なお、両社は、本剤を薬価収載後速やかに発売する予定であり、シェリング・プラウ株式会社からは「レメロン® (REMERON®)錠15mg」、明治製菓株式会社からは「リフレックス® (REFLEXR)錠15mg」の製品名のもと、2ブランド2チャンネルでのプロモーション活動を行ってまいります。
*注12007年11月19日N.V.オルガノン社はシェリング・プラウ・コーポレーションと統合
以上
ご参考
「ミルタザピン」の作用機序について
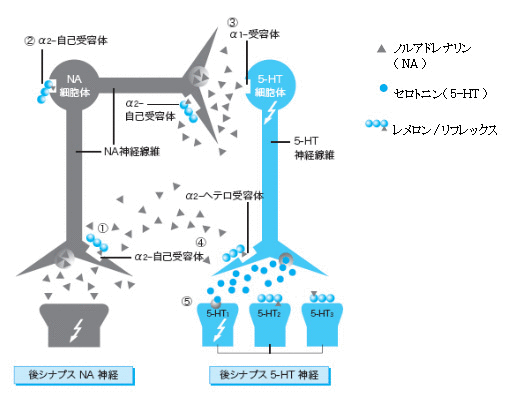
「ミルタザピン」は中枢神経のシナプス前α2-自己受容体およびヘテロ受容体に対して阻害作用を示し、中枢神経のノルアドレナリン(NA)およびセロトニン(5-HT)の神経伝達を増強します。セロトニン受容体に対して、「ミルタザピン」は5-HT2及び5-HT3受容体を阻害するため、抗うつ作用に関連する5HT1受容体を選択的に活性化させます。
(1)NA神経シナプス前α2-自己受容体を遮断することによりNA遊離を促進
(2)NA細胞体に存在するα2-自己受容体を遮断することによりNA神経を活性化
(3)NA遊離の促進による5-HT神経細胞体α1-受容体を介した5-HT神経活動の活性化
(4)5-HT神経シナプス前α2-ヘテロ受容体を遮断することにより5-HT遊離を促進
(5)後シナプス5-HT2,3受容体の拮抗作用
<レメロン® 錠 15mg/リフレックス® 錠 15mgの製品概要>
- 製品名:
- レメロン® 錠 15mg/リフレックス® 錠 15mg
(英文表記REMERON® tablets 15mg/REFLEX® tablets 15mg) - 一般名:
- ミルタザピン
(英文表記Mirtazapine) - 承認年月日:
- 2009年7月7日
- 効能・効果:
- うつ病・うつ状態
- 用法・用量:
- 通常、成人にはミルタザピンとして1日15mgを初期用量とし、15~30mgを1日1回就寝前に経口投与する。なお、年齢、症状に応じ1日45mgを超えない範囲で適宜増減するが、増量は1週間以上の間隔をあけて1日用量として15mgずつ行うこと。
- 製造販売元:
- シェリング・プラウ株式会社/明治製菓株式会社
