信頼性保証ポリシー私たちは、患者さんや医療関係者の皆様からの信頼を頂き、
社会に貢献してまいります。
Meiji Seika ファルマグループでは、上記の「信頼性保証ポリシー」を達成するために、各種法令や規範、並びにコンプライアンスを遵守した企業活動を行っています。そして、皆様にご提供する「製品」の信頼性を確保するために制定した「信頼性保証指針」を基に各グループ会社・部門の方針・基準を定め、これらをPDCAサイクルの活用により継続的に改善することで「製品」の信頼性の向上に取り組んでいます。この様な活動を通じて皆様からの信頼を頂き、社会に貢献してまいります。自社先発品はもとより、ジェネリック医薬品についても、このポリシーに従い、自社製造、委託製造問わず、同等の基準で運用しています。

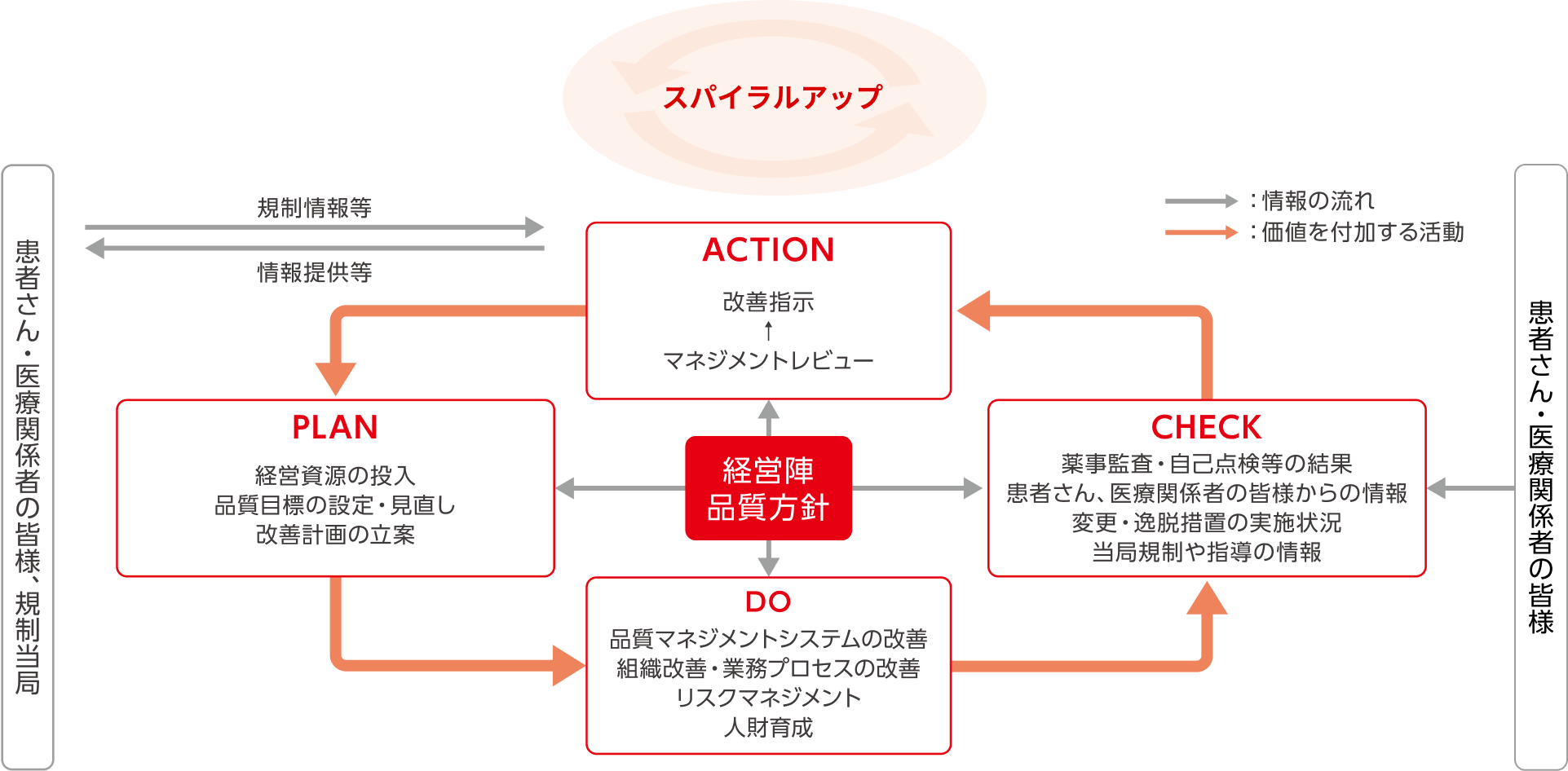
品質マネジメントシステムのPDCAサイクル
半年ごとの経営層へのマネジメントレビューにて実効性を評価し、更なる品質マネジメントシステムの向上を進めてまいります。
製造販売業体制
Me ファルマでは、製造販売業三役を設置し、三役が連携をとりながら品質確保に努めています。

Me ファルマ製品の品質保証体制
Meiji Seika ファルマグループでは、一貫した「meijiクオリティ」の基準のもと各社品質管理を行っています。
Me ファルマでは、Meiji Seika ファルマと連携した品質管理体制をとり、先発医薬品と同等の基準で管理されたジェネリック医薬品を販売しています。
品質管理強化の取り組み Meiji Seika ファルマグループでの製造品
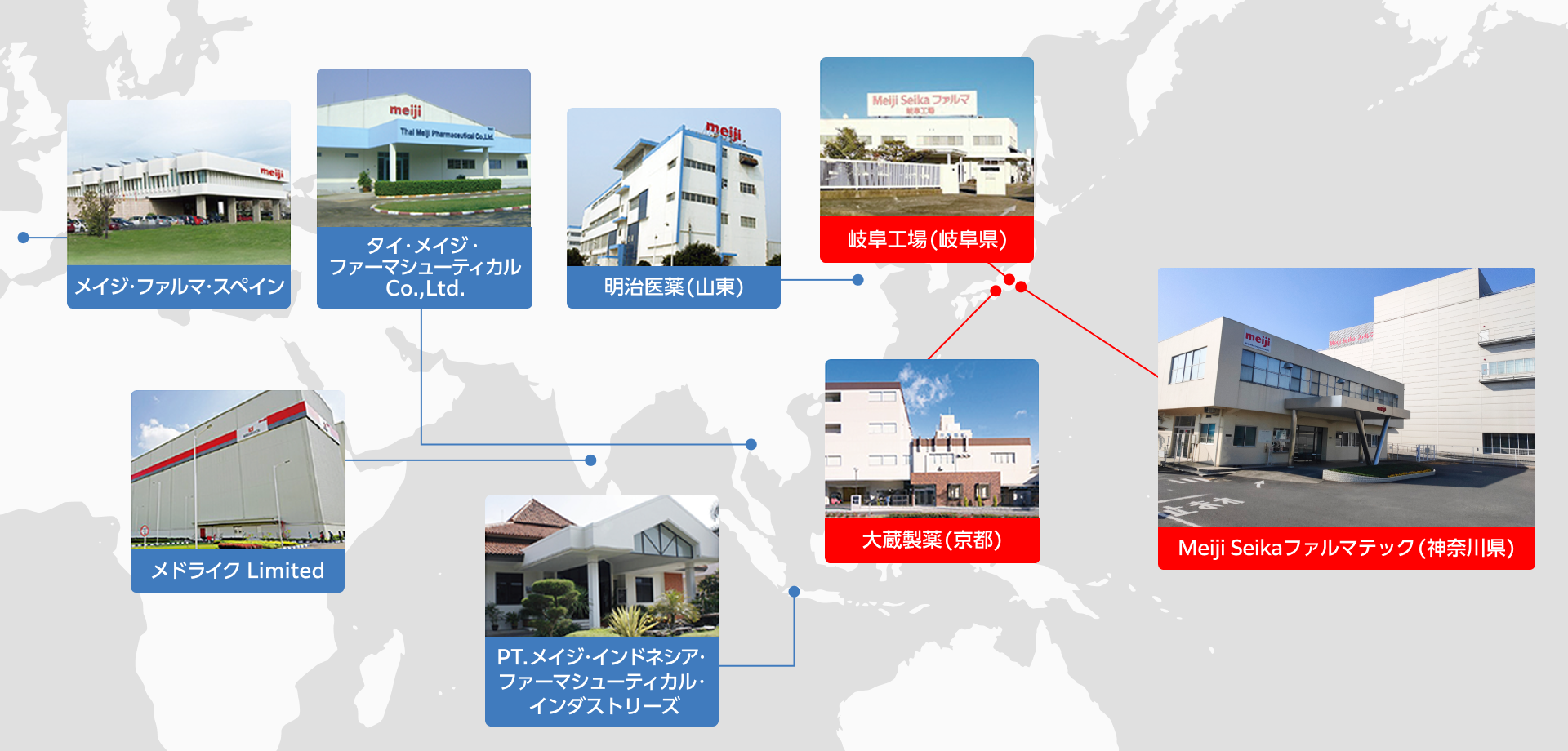
Meiji Seika ファルマグループは、世界各地に拠点をおき、生産体制を整備してきました。
Meiji Seika ファルマグループのこだわりは、製品の製造や品質の管理にかかわる様々な品質保証基準が先発医薬品、ジェネリック医薬品共に同等であることです。先発医薬品とジェネリック医薬品とで同等の基準で管理されている製造ラインを使用して質の高い医薬品を製造、出荷しています。
いずれの製造所も、GMPに則り、先発医薬品とジェネリック医薬品とで、同等の製造管理基準、品質管理基準にて医薬品を製造し出荷しています。
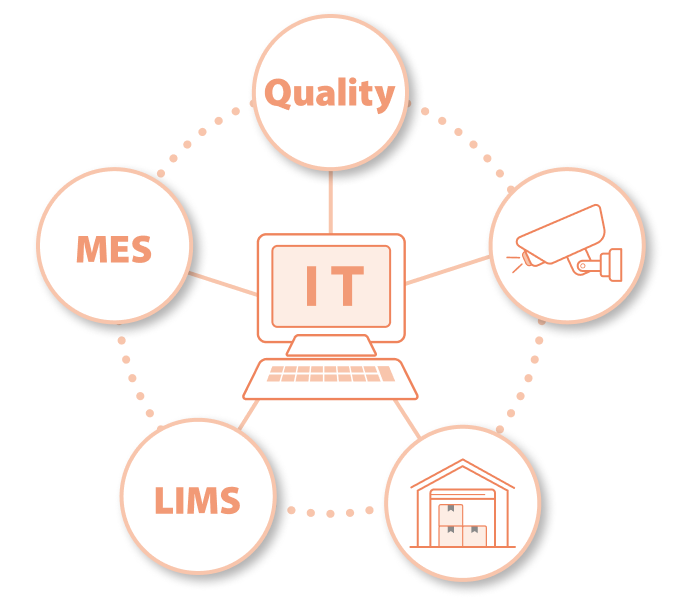
Meiji Seika ファルマテックの管理システム
MES、LIMS等のITを導入することにより、更に製品の信頼性を高める取り組みを進めていきます。
Meiji Seikaファルマテックでは製造工程を把握し作業者へ的確な指示を出して業務をサポートする「MES(製造実行管理システム)」と、品質検査情報を一元管理する「LIMS(ラボラトリー情報管理システム)」を導入しています。ITを駆使して生産の効率化を図るだけでなく、製造管理、品質管理の信頼を高める取り組みを行っています。
- 品質イベント管理システムの導入
- 製造実行管理システム(MES)の導入
- ラボラトリー情報管理システム(LIMS)の導入
- 倉庫管理システムの導入
- 監視カメラの導入
海外生産拠点の製造・品質管理の取り組み
日本の製造、試験に関するGMPを研修した現地スタッフが日本人スタッフの指導のもと、日本国内と同じ厳しい基準で製品の製造や品質の管理、製品試験を実施しています。製品はすべて日本で最終検査を行い、規格に適合していることを確認しています。

品質管理強化の取り組み 委託製造品
原薬および製剤の委託製造所についても、それぞれの製造管理基準、品質管理基準が「meijiクオリティ」を求めています。
委託製造品に対しては、Meiji Seika ファルマとの連携のもと、「承認書※1と製造実態の整合性確認強化」、「製造所監査の強化」に取り組んでいます。
委託製造所の定期監査の取り組み
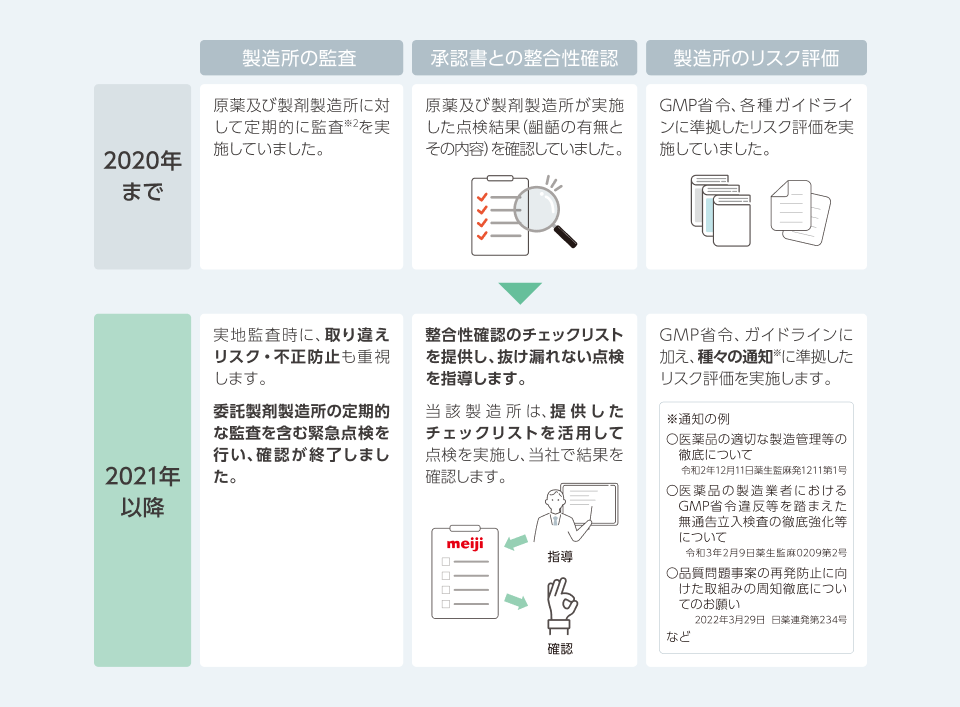
新規製造販売承認取得品の委託製剤製造所の監査
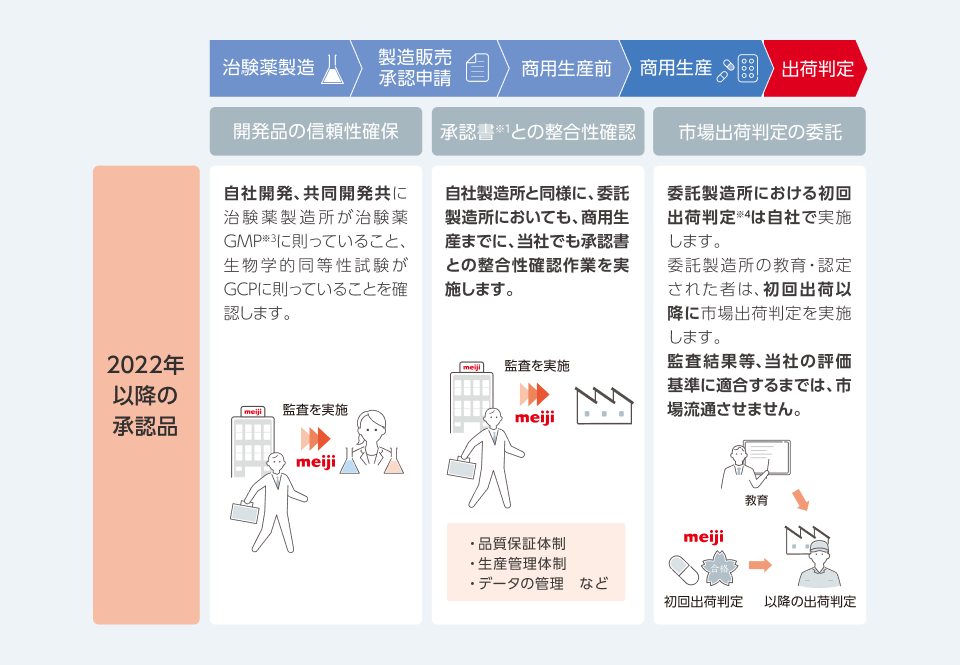
- ※1 承認前においては、承認書案。承認書案で監査した場合は、初回出荷判定時に承認書との齟齬を再度確認する。
- ※2 監査 : GQP省令、製造指図書、承認書に従って製造されたかどうかについて、製造販売業者が行う調査。
- ※3 治験薬GMP : GCP省令第17条1項及び第26条の3に規定される治験薬を製造する際に順守すべき適切な製造管理及び品質管理の方法並びに必要な構造設備にかかる事項を定めたもの。
-
※4
出荷判定 : 製品を市場に出荷する際、品質保証責任者が、製造の記録および品質試験の記録をチェックをし、出荷の可否を決定すること。
初回出荷判定の意義 : 新発売時においては、正しくシステムに則って、製造されているかの最終確認。
品質管理強化の取り組み 仕入品
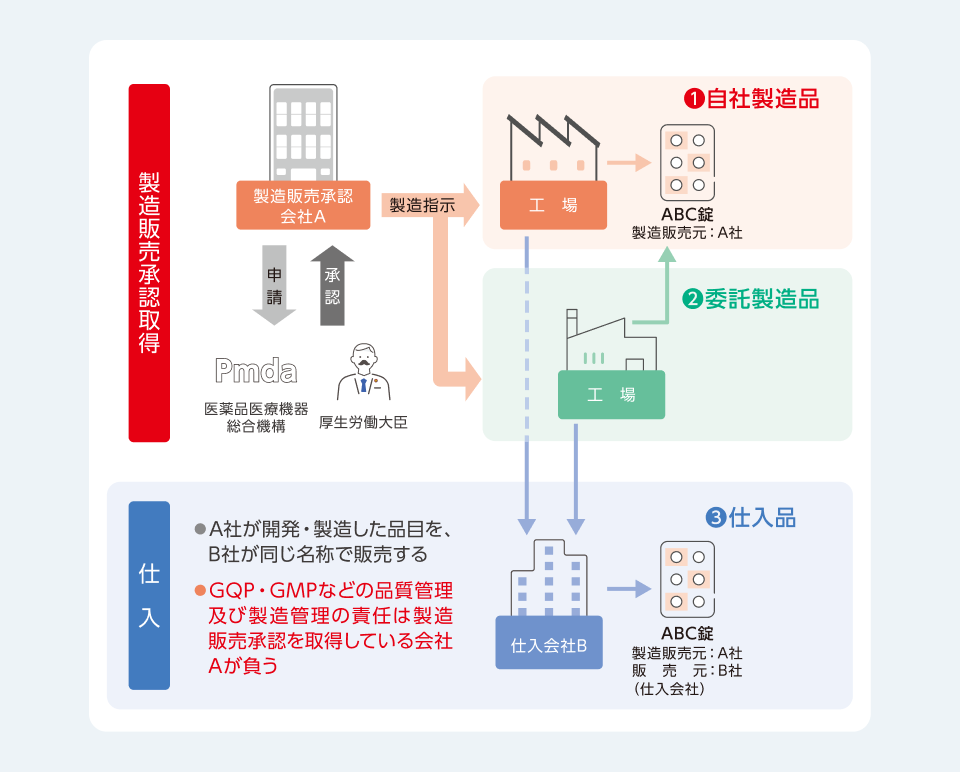
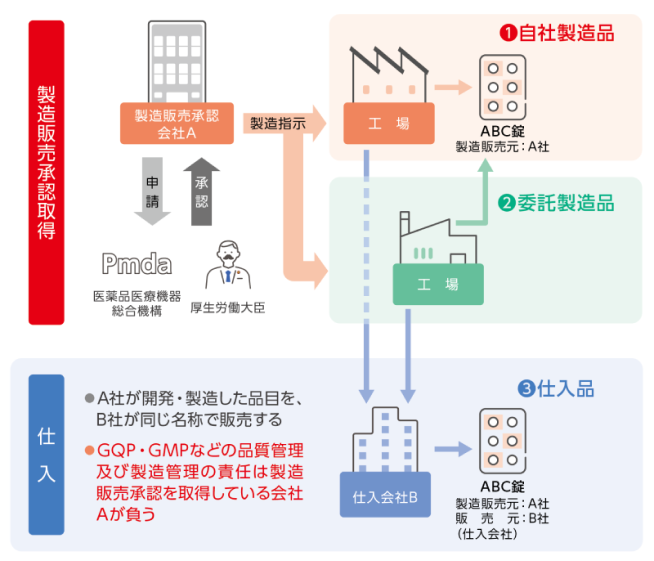
当社は信頼できる製造販売会社から製品を仕入れ、販売しています。
※仕入品:製造販売承認を取得することなく、他社が製造販売承認を有している医薬品を購入して販売する品目。
(参考)製造販売と仕入
情報公開
Me ファルマでは情報公開を進めています。
- 品質保証システムに対する取り組み
- ジェネリック医薬品の原薬製造国
- ジェネリック医薬品の製剤製造企業
- 製品の供給状況